| Mendeleev Communications |
|
|


|
|
|
Эта публикация цитируется в 10 научных статьях (всего в 10 статьях) Communications A novel urea derivative anticonvulsant: In vivo biological evaluation, radioreceptor analysis of GABAA receptors and molecular docking studies of enantiomers T. V. Shushpanovaa, N. A. Bokhanab, V. Yu. Kuksenokc, V. V. Shtrykovac, O. V. Shushpanovad, V. V. Udute a Mental Health Research Institute, Tomsk National Research Medical Center, Russian Academy of Sciences, Tomsk, Russian Federation b Siberian State Medical University, Tomsk, Russian Federation c National Research Tomsk Polytechnic University, Tomsk, Russian Federation d Scientific Center for Mental Health, Moscow, Russian Federation e E.D. Goldberg Scientific Research Institute of Pharmacology and Regenerative Medicine, Tomsk Research Center, Russian Academy of Sciences, Tomsk, Russian Federation 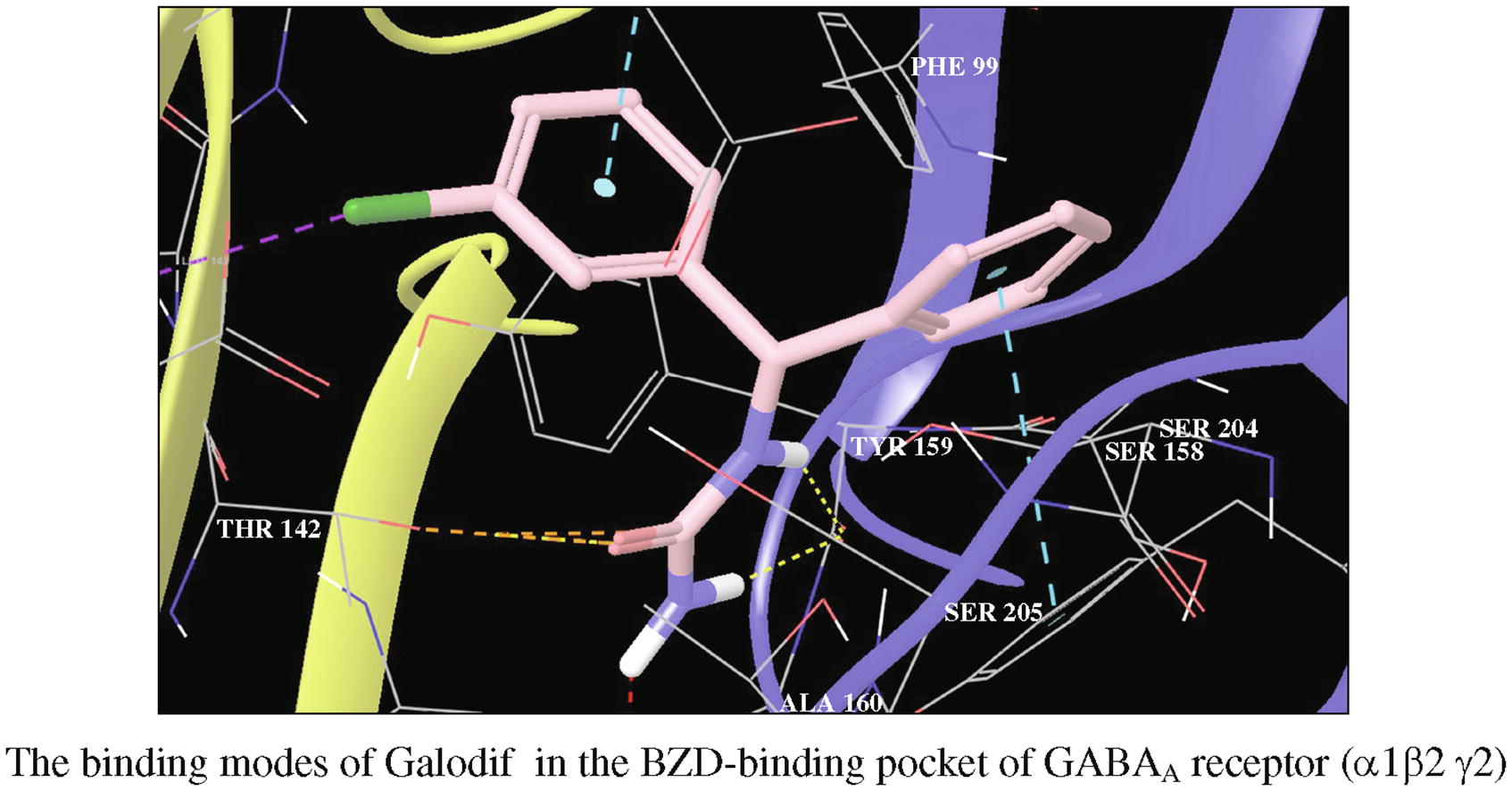
Образец цитирования: T. V. Shushpanova, N. A. Bokhan, V. Yu. Kuksenok, V. V. Shtrykova, O. V. Shushpanova, V. V. Udut, “A novel urea derivative anticonvulsant: In vivo biological evaluation, radioreceptor analysis of GABAA receptors and molecular docking studies of enantiomers”, Mendeleev Commun., 33:4 (2023), |

|

|
 Обратная связь:
Обратная связь: |
 Пользовательское соглашение Пользовательское соглашение
|
 Регистрация посетителей портала Регистрация посетителей портала |
 Логотипы Логотипы |
|










